![]()

免疫疗法的诞生和发展是本世纪癌症治疗领域里程碑式的进步[1],对于众多因传统治疗不耐受或无缓解而深陷绝望的患者来说,免疫疗法很有可能为他们提供一根新的救命稻草。免疫检查点抑制剂在免疫疗法中最富前景,已有数款免疫检查点抑制剂获批上市[2]。然而,由于免疫抑制性肿瘤微环境的存在以及肿瘤细胞与免疫系统间的相互作用,免疫检查点抑制剂的响应率仍然很低,只有20-30%的患者能从中获益[3]。肿瘤微环境由多种细胞组成,包括肿瘤细胞、调节性T细胞 (Treg)、成纤维细胞和肿瘤相关巨噬细胞 (TAM)等。TAM在瘤内含量丰富,占肿瘤质量的近50% [4],而且TAM的存在通常与肿瘤预后不良有关[6]。因此,重编程TAM细胞,以恢复其肿瘤杀伤功能引起了人们极大的兴趣,正发展为一种改善肿瘤免疫治疗效果的富有前景的新兴疗法[5]。

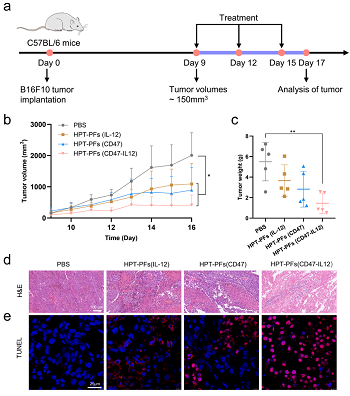
随后,作者通过一系列细胞水平实验,评估了HPT-PFs系统在体外递送基因的性能。与传统递送载体相比,HPT-PFs递送后CD47敲除率显著升高。同时,成功编辑的B16F10小鼠黑素瘤细胞能转化为IL-12生产工厂,并增强巨噬细胞对自身的吞噬。接着,团队通过皮下注射 B16F10细胞的方式构建了荷瘤小鼠模型,在体内证明HPT-PFs能显著抑制肿瘤生长(图2. a-c),并促进肿瘤细胞凋亡(图2. d,e)。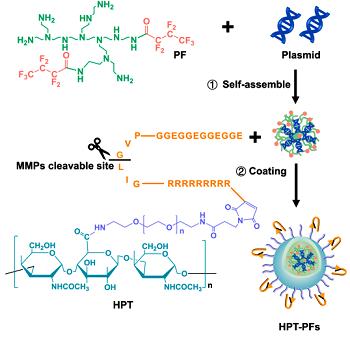
相关产品信息
一抗类
|
编号 |
英文名称 |
种属反应 (已验证) |
|
Rabbit Anti-CD31 pAb |
Hu,Mo,Rat,Rt |
|
|
Rabbit Anti-CD47 pAb |
Hu,Mo,Rat |
|
|
Rabbit Anti-CD86 pAb |
Hu,Mo,Rat |
|
|
Rabbit Anti-MRC1 (CD206) pAb |
Hu,Mo, Rat,Chi |
|
|
Rabbit Anti-MRC1 (CD206) pAb |
Mo |
|
|
Rabbit Anti-IFN gamma pAb |
Mo,Rat |
|
|
Rabbit Anti-IFN gamma pAb |
Hu |
|
|
Rabbit Anti-TNF alpha pAb |
Hu,Mo |
|
|
Rabbit Anti-TNF alpha pAb |
Hu |
其他类
|
编号 |
英文名称 |
|
DAPI solution (1mg/ml) |
|
|
DAPI solution (即用型) |
|
|
Goat Anti-rabbit IgG H&L/HRP |
|
|
Goat Anti-rabbit IgG H&L/AF594 |
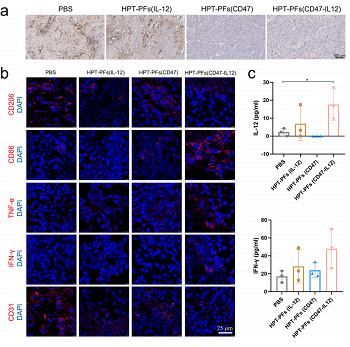
总的来说,本文作者开发的HPT-PFs (CD47-IL12)递送体系,能做到基于CRISPR原位高效地将癌细胞编辑为工程肿瘤细胞,增强TAMs吞噬能力并诱导TAMs从肿瘤支持性M2表型转变为肿瘤杀伤性M1表型,同时显著地抑制B16F10移植瘤在小鼠体内的生长。这一创造性工作为原位工程肿瘤细胞介导的免疫治疗开辟了一条新途径。考虑到多种肿瘤模型中TAMs的丰富性、免疫抑制机制的相似性及CRISPR系统操作的简易性,研究团队还将继续探索将这一系统应用于其他肿瘤免疫治疗场景的可能性,继续拓宽基于CRISPR的免疫治疗策略的适用范围。努力的汗水不应被一遍遍的重复实验所埋没,创意和灵感更加需要信得过的试剂给予支撑。给博奥森一份信任,我们还您的不只是一支好抗体!
参考文献
1.Meng L., Zhenzhen Y., et al. (2022). CRISPR-based in situ engineering tumor cells to reprogram macrophages for effective cancer immunotherapy. Nano Today, 32, 10359.
2.Menon, S., Shin, S., & Dy, G. (2016). Advances in Cancer Immunotherapy in Solid Tumors. Cancers, 8(12), 106.
3.Maleki Vareki, S., Garrigós, C., & Duran, I. (2017). Biomarkers of response to PD-1/PD-L1 inhibition. Critical reviews in oncology/hematology, 116, 116–124.
4.Cassetta, L., & Pollard, J. W. (2018). Targeting macrophages: therapeutic approaches in cancer. Nature reviews. Drug discovery, 17(12), 887–904.
5.Singh, Y., Pawar, V. K., Meher, J. G., et al. (2017). Targeting tumor associated macrophages (TAMs) via nanocarriers. Journal of controlled release : official journal of the Controlled Release Society, 254, 92–106.
6.Gajewski, T. F., Schreiber, H., & Fu, Y. X. (2013). Innate and adaptive immune cells in the tumor microenvironment. Nature immunology, 14(10), 1014–1022.
7.Yang, J., Zhang, Q., Chang, H., & Cheng, Y. (2015). Surface-engineered dendrimers in gene delivery. Chemical reviews, 115(11), 5274–5300.
8.Lv, J., Chang, H., Wang, Y., et al. (2015). Fluorination on polyethylenimine allows efficient 2D and 3D cell culture gene delivery. Journal of materials chemistry. B, 3(4), 642–650.
9.Wang, H., Wang, Y., Wang, Y., Hu, J., et al. (2015). Self-Assembled Fluorodendrimers Combine the Features of Lipid and Polymeric Vectors in Gene Delivery. Angewandte Chemie (International ed. in English), 54(40), 11647–11651.
10.Barberio, A. E., Smith, S. G., Correa, S., et al. (2020). Cancer Cell Coating Nanoparticles for Optimal Tumor-Specific Cytokine Delivery. ACS nano, 14(9), 11238–11253.
11.Voest, E. E., Kenyon, B. M., O'Reilly, M. S., et al. (1995). Inhibition of angiogenesis in vivo by interleukin 12. Journal of the National Cancer Institute, 87(8), 581–586.
Bioss 正在进行的促销活动
地 址: 北京市通州区马驹桥镇联东U谷西区四期67号楼 联系人: 秦 电 话: 4009019800 传 真: 010-58129612 Email:sales@bioss.com.cn
北京博奥森生物技术有限公司
商家主页
